Terminologie internationale des modalités de mesure des dimensions de la pièce d’electrorésection a l’anse diathermique pour le traitement des lésions intraépithéliales de haut grade du col utérin

Xavier CARCOPINO
Commentaire de l’article : Kyrgiou M et al. Terminology for cone dimensions after local conservative treatment for cervical intraepithelial neoplasia and early invasive cervical cancer. Lancet Oncol 2022; 23(8):e385-e392
L’électro résection à l’anse diathermique (ERAD) est aujourd’hui le traitement de référence pour la prise en charge des lésions intraépithéliales de haut grade du cancer du col de l’utérus. Ce geste combine l’avantage d’être très efficace, simple, de pouvoir être réalisé en ambulatoire sous anesthésie locale pour des couts limités. Il doit être systématiquement réalisé sous guidage colposcopique direct afin de permettre une résection optimale, combinant à la fois un volume et une hauteur de résection contenus et une exérèse complète, idéalement en marges saines.1,2 L’impact de ce type de traitement sur une grossesse ultérieur est maintenant bien connu. Ces patientes sont exposées à un risque accru d’accouchement prématuré, parfois sévère.3 Plusieurs éléments sont déterminants pour le risque d’accouchement prématuré ultérieur dont la hauteur de l’exérèse réalisée ainsi que le volume de col retiré.3–6 Ainsi, le risque d’accouchement prématuré est directement lié à l’importance de l’exérèse réalisée et augmente proportionnellement avec la hauteur de l’exérèse réalisée.3
La mesure précise des dimensions de la pièce opératoire d’ERAD est de ce fait un élément important pour le suivi ultérieur des patientes et la caractérisation du risque de prématurité secondaire. A ce jour, s’il est admis que ces mesures doivent figurer de façon systématique dans le compte rendu histologique, il n’existe aucun consensus sur les modalités précises de prise de ces mesures. Initialement, l’International Federation of Colposcopy and Cervical Pathology (IFCPC) a proposé de mesurer la longueur, la circonférence et l’épaisseur de la pièce opératoire, mais ces recommandations n’ont à ce jour pas été suivies et ne font pas consensus.6–8 Cette publication présente les recommandations internationales jointes de l’European Society of Gynecology and Oncology (ESGO), de l’European Federation for Colposcopy (EFC), de l’IFCPC et de l’European Society of Pathology (ESP) qui sont arrivées à un consensus sur les modalités de mesure des dimensions et du volume de la pièce opératoire d’ERAD.9
Ainsi, les mesures admises de la pièce opératoire d’ERAD sont le diamètre antéro-postérieur, le diamètre transverse et la longueur (Figure 1). Elles doivent être exprimées en mm et apparaître dans cet ordre donné. Le diamètre antéro-postérieur correspond à la distance entre la marge de résection antérieure et la marge de résection postérieure. Le diamètre transverse correspond à la distance entre la marge de résection droite et la marge de résection gauche. Enfin, la longueur correspond à la distance entre l’orifice cervical externe et la limite endocervicale de la résection. L’orientation de la pièce est recommandée et doit se faire par la mise en place d’un fil repère à midi, sans ouvrir la pièce opératoire. Enfin, il est précisé que dans le cas où la pièce opératoire ne serait pas orientée, ces diamètres doivent être choisis de façon aléatoire.
Le volume de la pièce d’exérèse doit également être renseigné, idéalement par le biais de la méthode du déplacement de fluide par immersion complète de la pièce opératoire dans un verre gradué. Mais celui-ci peut également être mesuré directement à partir des dimensions de la pièce d’ERAD à partir de la formule suivante :
Volume = (p/6) x diamètre antéro-postérieur x diamètre transverse x longueur
Enfin, il est à noter que le moment de prise de ces mesures compte puisque l’immersion dans le formol à 4 % provoque la rétraction des tissus d’environ 0 à 3 %. On notera que la rétraction des tissus est quasiment nulle lorsque la pièce est placée dans une solution de formol à 4 % à 37 °C alors qu’elle est de 3 % si le formol est à température ambiante (25 °C).10
Cette nouvelle terminologie est simple et facilement applicable. Elle permet une standardisation des mesures, l’extrapolation des résultats des études à la pratique clinique et l’harmonisation des données. Il est important qu’elle soit utilisée dès à présent et que ces données figurent systématiquement dans les comptes rendus histologiques de l’analyse des pièces d’ERAD.
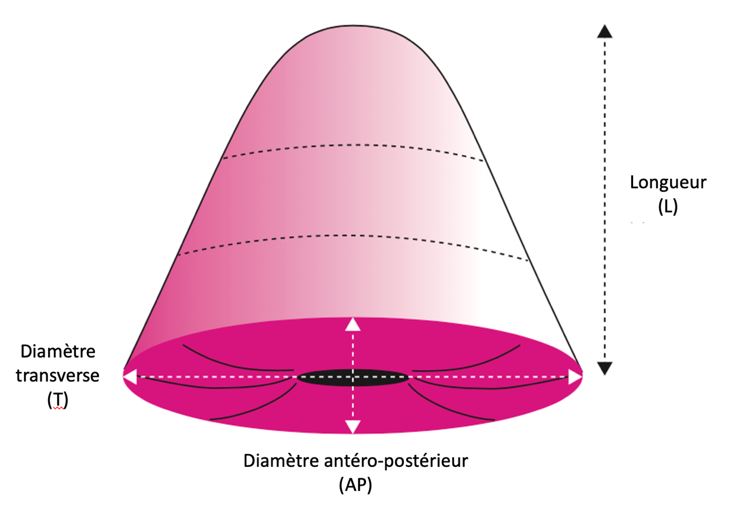
Figure 1. Modalités de mesures des dimensions de la pièce opératoire d’ERAD
BIBLIOGRAPHIE
1. INCA. Conduite à tenir devant une femme ayant une cytologie cervico-utérine anormale - Thésaurus. (2017).
2. Preaubert, L. et al. Benefits of Direct Colposcopic Vision for Optimal LLETZ Procedure: A Prospective Multicenter Study. J Low Genit Tract Dis 20, 15–21 (2016).
3. Kyrgiou, M. et al. Adverse obstetric outcomes after local treatment for cervical preinvasive and early invasive disease according to cone depth: systematic review and meta-analysis. BMJ 354, i3633 (2016).
4. Founta, C. et al. Proportion of excision and cervical healing after large loop excision of the transformation zone for cervical intraepithelial neoplasia. BJOG 117, 1468–1474 (2010).
5. Kyrgiou, M. et al. Obstetric outcomes after conservative treatment for cervical intraepithelial lesions and early invasive disease. Cochrane Database Syst Rev 11, CD012847 (2017).
6. Khalid, S. et al. The thickness and volume of LLETZ specimens can predict the relative risk of pregnancy-related morbidity. BJOG 119, 685–691 (2012).
7. Carcopino, X. et al. Image assessment of cervical dimensions after LLETZ: a prospective observational study. BJOG 120, 472–478 (2013).
8. Carcopino, X. et al. The Accuracy of Large Loop Excision of the Transformation Zone Specimen Dimensions in Determining Volume: A Multicentric Prospective Observational Study. J Low Genit Tract Dis 21, 120–124 (2017).
9. Kyrgiou, M. et al. Terminology for cone dimensions after local conservative treatment for cervical intraepithelial neoplasia and early invasive cervical cancer: 2022 consensus recommendations from ESGO, EFC, IFCPC, and ESP. Lancet Oncol 23, e385–e392 (2022).
10. Fox, C. H., Johnson, F. B., Whiting, J. & Roller, P. P. Formaldehyde fixation. J Histochem Cytochem 33, 845–853 (1985).







