Optimiser le dépistage du cancer du col de l’utérus chez les patientes ayant beneficié de la vaccination anti-hpv

Marine JOSTE
Article commenté : Canfell K, Caruana M, Gebski V, Darlington-Brown J, Heley S, Brotherton J, et al. Cervical screening with primary HPV testing or cytology in a population of women in which those aged 33 years or younger had previously been offered HPV vaccination: Results of the Compass pilot randomised trial. PLoS Med. 2017;14:e1002388 [1].
Auteurs : Marine Joste & Jean Levêque
Dpt de Gynécologie Obstétrique et Reproduction Humaine. CHU Anne de Bretagne – Rennes
__________________________________________________________________________________
Le travail présenté dans cet article concerne un essai randomisé sur le dépistage cytologique versus virologique chez des femmes vaccinées et non vaccinées en Australie.
L'Australie se distingue par la qualité de sa médecine préventive comme en témoigne le fort taux de couverture vaccinale HPV (chez les 12-13 ans, 2 doses : 83% et 3 doses : 77%) et son dépistage des pathologies cervicales reposant sur la réalisation d'un test virologique (test avec génotypage partiel (HPV 16 et 18, et autres HPV haut risque : Cobas 4800®) chez les 25-69 ans tous les 5 ans.
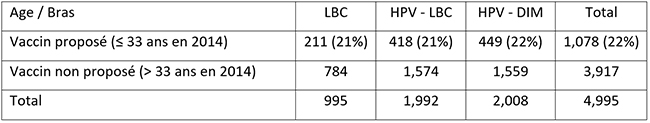
L'essai Compass a randomisé des patientes en 3 bras (1 : 2 : 2) : cytologie Liquid Based Cytology – LBC, Virologie (Cobas 4800®) et triage par LBC, Virologie (Cobas 4800®) et triage par double immunomarquage (DIM : par CINTec®) chez des patientes à qui a été proposée la vaccination (≤ 33 ans en 2014) ou non (> 33 ans en 2014) en intention de traiter (Tableau 1).
Tableau 1. Répartition des patientes selon l'âge éligible pour la vaccination
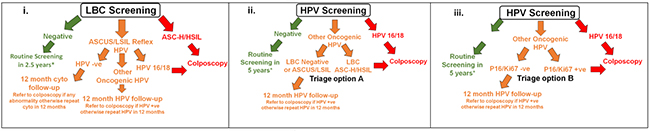
La prise en charge des 3 groupes restait proche de ce qui est proposé en France aux patientes ayant un frottis et aux patientes bénéficiant d'un dépistage virologique dans les pays le pratiquant (Figure 1).
Figure 1. Management des patientes dans les 3 groupes (cytologie, HPV et triage par cytologie, HPV et triage par DIM)
Dans le groupe LBC, le taux de cytologie de haut grade (H-SIL et ASC-H) était de 0.1%, de bas grade (ASC-US et L-SIL) de 6.6% avec une virologie de triage négative de 66.7%.
Dans le groupe HPV-LBC, 1.3% des participantes étaient HPV(16, 18) +, 5.5% étaient hr-HPV + (non 16 et non 18) parmi lesquelles 13.8% avaient une cytologie de haut grade et ont donc bénéficié d'une colposcopie.
Dans le groupe HPV-DIM, 1.1% des participantes étaient HPV(16, 18) +, 6.0% étaient hr-HPV + (non 16 et non 18) parmi lesquelles 26.9% avaient un DIM positif et ont donc bénéficié d'une colposcopie.
Les principaux résultats sont résumés sur le tableau 2.
Tableau 2. Principaux résultats de l'essai COMPASS
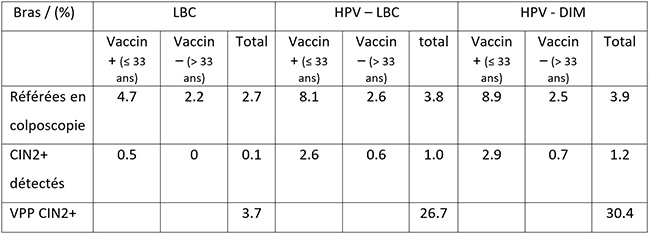
On retrouve dans cet article la notion d'une meilleure sensibilité du dépistage virologique versus cytologique (sensibilité relative de 1.27 [95%IC : 1.06-1.52] dans la méta-analyse d'Arbyn [2], mais aussi et pour la première fois dans le cadre d'un essai randomisé dans une population avec un taux de couverture vaccinale élevée lors du premier round du dépistage. Le deuxième point important est la preuve de l'efficacité de la complémentarité entre prévention primaire (vaccination contre HPV 16 et 18) et secondaire (dépistage virologique utilisant un test de génotypage partiel différenciant HPV 16 & 18, des autres HPV haut risque) : le taux de patientes les plus jeunes (25-34 ans) référées en colposcopie à l'issue immédiate du test de dépistage (donc le COBAS 4800 positif à HPV 16 et/ou 18 [3]) dans les bras utilisant un test virologique (2%) n'est pas significativement différent du taux historique observé en Australie (1.5%) confortant le choix d'un algorithme de triage à 2 étages (HPV 16 / 18 positif = colposcopie, et présence d'un HPV non 16 / non 18 = contrôle à 1 an d'une cytologie négative ou de bas grade).
L'utilisation du DIM est une option intéressante qui a été retenue dans les dernières recommandations de l'INCa en option de triage dans les frottis de bas grade ASC-US et L-SIL : dans l'étude COMPASS le DIM est responsable d'une inflation de colposcopies initiales (prêt de 50% de colposcopies en plus, mais il n'existe plus de différences en termes de taux de colposcopie sur les 12 mois de l'étude entre le bras HPV-LBC et le bras HPV-DIM. Le deuxième point d'intérêt du DIM est qu'il rend possible une automatisation de la lecture.
Au total, cette première étude australienne est un plaidoyer pour considérer le dépistage virologique dans les populations vaccinées et doit servir de base de réflexion en France pour une organisation et articulation efficaces de la prévention primaire et secondaire.
Références
[1] Canfell K, Caruana M, Gebski V, Darlington-Brown J, Heley S, Brotherton J, et al. Cervical screening with primary HPV testing or cytology in a population of women in which those aged 33 years or younger had previously been offered HPV vaccination: Results of the Compass pilot randomised trial. PLoS Med. 2017;14:e1002388.
[2] Arbyn M, Ronco G, Anttila A, Meijer CJ, Poljak M, Ogilvie G, et al. Evidence regarding human papillomavirus testing in secondary prevention of cervical cancer. Vaccine. 2012;30 Suppl 5:F88-99.
[3] Wright TC, Stoler MH, Behrens CM, Sharma A, Zhang G, Wright TL. Primary cervical cancer screening with human papillomavirus: end of study results from the ATHENA study using HPV as the first-line screening test. Gynecol Oncol. 2015;136:189-97.







